DE L'IDENTIFICATION ET SIGNALEMENT DES EFFETS SECONDAIRES À L'AUTOSURVEILLANCE
L’IPC a souhaité donner une réalité concrète au concept de démocratie sanitaire, en stimulant la participation des patients à la surveillance de leurs chimiothérapies en tant que « co-acteurs » de leurs soins, leur donnant autonomie et indépendance à travers une surveillance « pro-active » des produits reçus, en les invitant à s’associer au repérage, au signalement et à la prise en charge des effets secondaires de ces thérapeutiques. Pour ce faire un programme d’accompagnement à la déclaration en ligne des EI sur le site de l’ANSM leur a été proposé depuis octobre 2015, avec l’aide d’un personnel infirmier formé.
De plus, ont été associés des patients du Comité de patients ainsi que des membres du milieu associatif aux côtés du personnel infirmier. Ils sont présents dans les espaces d’attente des lieux de consultation au contact des patients pour les aider dans cette démarche.
Cette démarche a été accompagnée par une formation réalisée par des experts en pharmacovigilance.
Après un an et demi de cette expérimentation 138 déclarations d’effets secondaires ont été effectuées par les patients sur le site de l’ANSM, avec l’aide d’une infirmière ou pour 30 % d’entre elles avec l’aide d’un bénévole (ainsi 42 déclarations d’EI de patients allogreffés ont été réalisées par des bénévoles formés de l’association RESTART). Ces déclarations ont été effectuées dans le cadre d’une prise en charge ambulatoire, dans l’enceinte de l’hôpital.
Ce niveau quantitatif de déclarations (138 sur une période de 18 mois) est à mettre en parallèle avec les chiffres nationaux de déclarations par des patients atteints de cancers. En effet, les données issues de la base nationale de pharmacovigilance qui totalise seulement 215 déclarations effectuées en 4 ans par les patients concernant les traitements du cancer (38 en 2012, 49 en 2013, 53 en 2014 et 75 en 2015).
Parmi ces déclarations réalisées à l’IPC, 74 concernent des thérapies ciblées (52 %), 42 déclarations des traitements utilisés après greffes (immunosuppresseurs, anti-infectieux).
Ces déclarations sont pertinentes et peu de demandes d’informations complémentaires ont été effectuées par le centre régional de pharmacovigilance.
La majorité des effets indésirables déclarés par les patients (65 %) impactent la qualité de vie et ont des conséquences sur leur vie quotidienne (qui peut aller jusqu’à un arrêt de travail pour certains d’entre eux). Pour 34 patients, cet impact est exprimé comme un isolement social, familial ou psychologique (impossibilité de sortir de chez soi, de marcher, de conduire, de communiquer, etc).
Les effets secondaires les plus cités concernent la peau, les phanères, puis viennent les neuropathies, paresthésies, crampes, tremblements, la fatigue, les douleurs quelle que soit leur origine, les troubles digestifs, les troubles liés à l’alimentation (prise ou perte de poids, problème d’alimentation, de goût), les troubles de la vue et de l’audition et la dépression/anxiété.
Il est important de noter que 3 pathologies cancéreuses secondaires ont été déclarées par les patients (cancer des testicules, carcinome épidermoïdes et cancer de la vessie).
Ce programme a aussi eu des résultats « collatéraux » au sein de l’IPC. En effet, il a eu un impact positif sur la notification des EI par les professionnels de santé eux-mêmes : celles-ci sont passées de 30 en 2014, 73 en 2015 puis à 100 en 2016).
Il est encore trop tôt pour pouvoir extrapoler à partir de cette expérimentation, en cours, que veut être l’impact de l’auto surveillance et de la déclaration par les patients sur la pharmacovigilance des anti- cancéreux.
Néanmoins les bénéfices de cette approche sont potentiellement multiples : bénéfice collectif, en permettant de mieux connaître la tolérance des médicaments en élargissant le périmètre de surveillance, prenant en compte le vécu direct des patients – et favorisant donc directement le « bon usage » du médicament dans « la vraie vie » en toute transparence – ; bénéfice individuel, puisqu’elle permet au patient, « signalant » aux autorités – et aussi , avant tout à son médecin – , de prévenir des conséquences potentiellement lourdes sur sa qualité de vie… voire liées à une mauvaise observance du traitement de sa pathologie.
La participation active des patients atteints de cancer à la surveillance de leur traitement correspond à une demande croissante et légitime d’information et d’autonomie, et permet une pratique concrète et légitime de « démocratie participative de proximité ».
L’expérience montre que cette approche est pertinente et réaliste moyennant un engagement symétrique et réactif des professionnels. De plus elle souligne la faisabilité et l’intérêt d’associer des « patients témoins-experts » à cette démarche.
La pharmacovigilance
De la théorie à la pratique
Ségolène DURAN, Pharmacienne, référent interne en pharmacovigilance à l’IPC
Identification et signalement des effets secondaires
Tous les médicaments peuvent avoir des effets secondaires dont la déclaration aux autorités sanitaires, publiques et indépendantes, permet de surveiller l’usage d’un médicament dans la population et de prévenir d’éventuelles complications liées au produit, éventuellement sous-estimées voire non connues.
C’est le rôle donné en France au système national de pharmacovigilance qui repose notamment sur l’analyse des notifications spontanées faites par les professionnels de santé. Il est similaire dans la plupart des pays européens et aux États-Unis.
La sous-déclaration des effets indésirables reste fréquente, parfois estimée à près de 90 % (moins de 10 % des EIG sont notifiés spontanément et moins de 5 % des EI non graves ). Elle est particulièrement marquée (et marquante, voire pénalisante) en cancérologie.
Même si les déclarations des cas d’effets indésirables dans le système national de pharmacovigilance sont en constante augmentation – passant de 23 936 en 2008 à 47 089 en 2015 -, il reste encore à grandement améliorer les signalements de pharmaco-vigilance, et notamment en cancérologie. En 2015, si l’ANSM avait reçu 38 779 nouvelles déclarations de pharmacovigilance, seulement 6 242 concernaient des médicaments anti cancéreux (soit 13 % du total des déclarations).
Et pourtant ces produits ne sont pas réputés pour leur bonne tolérance…
Plusieurs raisons sont généralement évoquées pour expliquer cette sous-déclaration, raisons qui sont le plus souvent associées :
- arbitrage difficile sur ce qu’il faut déclarer, les effets secondaires des anti-cancéreux étant fréquents, souvent majeurs et « attendus »,
- rapport bénéfice/risque étroit des traitements cytostatiques
- comorbidités importantes pouvant rendre difficile le diagnostic différentiel avec un éventuel effet indésirable lié au médicament et captant souvent toute l’attention du personnel soignant,
- lourdeur bureaucratique de la déclaration,
- réserves sur l’intérêt pour le patient et la collectivité par manque de retour d’information aux déclarants
- accoutumance aux effets secondaires (et au risque), passée la phase initiale d’utilisation d’un nouveau produit et l’ « effet notoriété » qui l’accompagne,
- crainte de judiciarisation de la relation soignant-soigné.
Depuis la loi du 10 juin 2011, les patients peuvent, directement auprès de l’ANSM, déclarer tout événement indésirable, qu’il soit grave ou non, attendu ou non. Pourtant, la proportion de déclarations effectuées par les patients évolue peu, passant entre 2012 et 2015 de 3 % à seulement 5 % de toutes les déclarations. Si on examine spécifiquement la situation des anticancéreux, la faible participation des déclarations de patients est particulièrement notable. Ainsi, en 2015 sur 6 242 déclarations liées à ces classes de produits, 75 seulement émanaient de patients.
Il semble donc que, malgré les informations données, en particulier par les associations de malades (dont la Ligue contre le cancer qui a ouvert sur son site un accès à la déclaration en ligne), cette possibilité n’ait pas réellement été connue ni saisie par les patients. Une des raisons évoquées de cet « échec » est le manque d’information donnée directement aux patients, ainsi que le manque de sensibilisation sur l’utilité de déclarer.
Cette situation pose problème, notamment pour mesurer de manière adéquate la balance bénéfice/risque des médicaments anticancéreux, et surtout son évolution au cours du temps, aussi bien à l’échelle collective que dans la parcours thérapeutique d’un malade.
Pourquoi l'autosurveillance ?
Pourquoi l’auto-surveillance ?
Parce que la prise en charge du cancer évolue…
Les données issues des essais cliniques étant utilisées essentiellement pour l’enregistrement des molécules, très peu d’informations sont disponibles lors de l’utilisation de ces molécules dans la « vraie vie » après l’AMM, spécialement en matière de tolérance.
Cette situation se retrouve fréquemment avec les nombreuses nouvelles molécules utilisées dans le traitement des cancers, qui font souvent l’objet de procédures accélérées d’enregistrement autorisant une mise sur le marché rapide (En 2015 plus de 500 molécules anti-cancéreuses sont en cours de développement à visée potentielle d’enregistrement par les Autorités sanitaires de régulation). Dans ces cas, on dispose de peu de recul sur leur utilisation à grande échelle, chez des patients non sélectionnés souvent poly-médicamentés.
Par ailleurs, dans un contexte de chronicisation de certaines maladies cancéreuses, ces molécules sont souvent utilisées pendant de longues périodes, administrées par voie orale chez des malades qui passent une grande partie de leur temps de traitement à leur domicile. Les données de la « situation de la chimiothérapie des cancers en France » mettent en évidence une activité de chimiothérapie toujours croissante et en mutation du fait du développement particulier des chimiothérapies par voie orale et en particulier dans le cadre des efforts pour déployer une « médecine de précision ». Ceci est corrélé avec les dépenses en molécules classiques dites cytotoxiques qui ont diminué au profit des thérapies ciblées au fil du temps.
Cette évolution des modalités de prise en charge expose les patients à des risques de toxicité non seulement à court terme, mais également à moyen-long terme, toxicités qui ne sont pas détectées durant le développement de la molécule et que la patient « expérimentera » probablement « hors les murs » de l’hôpital.
De plus, les nouvelles thérapies du cancer appartiennent fréquemment à de nouvelles classes thérapeutiques, dites de biothérapie, notamment les anticorps monoclonaux, les cytokines et les petites molécules inhibitrices de kinases impliquées dans la prolifération cellulaire. Les effets secondaires de ces biothérapies diffèrent notablement des effets dits « classiques » et souvent spectaculaires des chimiothérapies cytotoxiques, justifiant en soi une attention particulière et personnalisée par les acteurs de ces traitements, incluant autant que possible les patients eux-mêmes.
Parce que la déclaration faite par le patient est complémentaire et précise…
Inclure le patient dans la déclaration des effets secondaires se justifie également par les résultats de plusieurs études ayant démontré l’existence d’une discordance entre les effets indésirables (EI) déclarés par les médecins, et ceux déclarés par les patients, y compris dans le traitement du cancer. Les EI notifiés par les malades sont souvent différents de ceux qui le sont par les professionnels de santé. Ils sont plus habituellement d’ordre qualitatif ou fonctionnel. Ils portent aussi souvent sur les problèmes pratiques qu’entraînent la prise du médicament et son retentissement sur la vie quotidienne, là où les médecins déclarent davantage les EI qu’ils considèrent comme pouvant mettre en danger le patient, voire le pronostic vital.
D’autre part, les déclarations faites par les patients ont permis de mettre en évidence des toxicités jusqu’alors non recensées (notamment par les médecins) de certains médicaments (effets inattendus) comme cela a pu être le cas dans le VIH concernant les troubles de la libido. L’importance de la déclaration des patients est confirmée dans une analyse de la base nationale de pharmacovigilance anglaise qui souligne la complémentarité des déclarations effectuées par les patients à celles effectuées par les professionnels de santé :
Il est aussi noté que cette approche permet la détection de nouveaux effets secondaires, est associée à une description plus détaillée et plus précise des EI ayant des conséquences sur la vie quotidienne.
Parce qu’elle a un impact positif sur la qualité de vie des patients et la réponse au traitement…
Selon plusieurs études : l’intégration par le médecin en temps réel des données reportées par le patients (dont les EI) peut améliorer le qualité de vie des patients, la communication avec leur médecin, réduire le recours à un service d’urgence et allonger la survie.
Parce que les patients souhaitent s’impliquer…
Dans d’autres contextes, et notamment en France à l’occasion de la pandémie grippale H1N1 de l’hiver 2009-10, il a pu être montré que les patients étaient mobilisables pour faire des déclarations d’effets secondaires, déclarations non seulement riches sur le plan quantitatif* mais pertinentes sur le plan de la sécurité sanitaire.
Parce que d’autres pays l’utilisent efficacement dans leur système de pharmacovigilance…
C’est le cas en Angleterre, notamment à travers la « yellow card » ; les déclarations des patients y sont devenues un élément important de la pharmacovigilance nationale à la fois sur le plan quantitatif mais aussi qualitatif.
C’est aussi maintenant le cas dans de nombreux autres pays : sur 50 pays étudiés depuis 2000, le nombre médian d’EI rapportés par an est de 3 678 (de 132 en Estonie à 874 116 aux USA), avec un maximum de 3 700 déclarations par an et par million d’habitants pour la Grande-Bretagne.
Parce que ces effets secondaires ont un impact sur l’observance au traitement…
Les travaux précurseurs dans le domaine du VIH avaient mis en évidence l’impact des symptômes ressentis sur l’observance des patients, ce qui peut constituer une perte de chance pour le patient. A ce titre, il paraît intéressant d’évaluer les conséquences que peuvent avoir sur l’observance ces déclarations d’EI. L’hormonothérapie des cancers du sein, un traitement aux effets majeurs sur la survie, en est un second exemple : plusieurs études en population montrent que plus de 25 % des patientes abandonnent le traitement après 3 ans, du fait d’effets secondaires peu spectaculaires pour les soignants mais invalidants pour la malade, des abandons qui éventuellement ne sont pas signalés au médecin…
Parce les effets secondaires ressentis par les patients sont insuffisamment pris en compte dans la « vraie vie »…
Si la discordance entre médecins et malades dans la nature et la fréquence de signalement des effets secondaires des traitements a été largement étudiée dans le cadre des essais cliniques, peu de travaux ont porté sur de telles évaluations en pratique clinique courante.
Ces différences de perception ont été retrouvées dans la leucémie myéloïde chronique où la sévérité des symptômes déclarés par le patient est plus importante que celle déclarée par les médecins pour des effets « subjectifs » comme la fatigue. Intégrer les effets secondaires rapportés par les patients dans leur prise en charge devrait permettre de l’améliorer.
Parce que les forums santé et autres recherches sur internet deviennent de nouveaux outils d’expression mais aussi de surveillance des besoins des patients…
La FDA a ainsi mis en place un partenariat avec un forum internet de patients (patientslikeme) pour récupérer des EI directement des patients intégrés dans le système national américain de pharmacovigilance.
L’ANSM soutient plusieurs études de recherche – en cours – analysant l’impact des réseaux sociaux sur la surveillance des produits de santé.
*900 fiches de déclaration avaient ainsi pu être ainsi collectées, soit environ 20 % du total des signalements concernant les effets indésirables des vaccins et des antiviraux utilisés pendant cette période
Expérience-pilote de l’IPC
La chirurgie oncologique mammaire, et plus particulièrement la chirurgie reconstructrice, notre domaine d’activité, est un domaine où le recueil des PROs est particulièrement adapté, par la place centrale qu’y tient la mise en place de prothèses mammaires en silicone (PMS). Ces dispositifs médicaux implantables sont, en effet, à haut risque d’effets indésirables, du fait de leur durée de vie limitée, de la topographie et du caractère invasif de leur implantation.
Ceci, rajouté à leur très large diffusion (en France, depuis 2001, environ 340 000 femmes en portent ou en ont porté) fait de la surveillance des PMS une priorité sanitaire (rapport ANSM, sept 2012).
Les effets secondaires (ES) pouvant apparaître tout au long de la durée de vie d’une PMS, et les patientes étant vues de loin en loin par les médecins après la phase initiale de surveillance rapprochée, il paraît logique qu’une partie importante de cette surveillance pro-active leur soit confiée.
Ceci est d’autant plus vrai que dans une étude-pilote réalisée à l’IPC, nous avons montré que la consultation systématique des patientes sur leur vécu permettait de donner une appréciation plus complète des effets secondaires. En effet, après la mise en place, en mars 2015, d’un plan d’action visant à prendre en compte la totalité des événements ressentis par les patientes, après pose de PMS, nous avons constaté une augmentation quantitative et qualitative des signalements d’ES :
Entre la période 2010-2014 (« avant » le début du plan d’action), et la période 2014-2015 (« après » le début du plan d’action) le nombre de signalements est passé de 60 en 4 ans à 38 sur une seulement en 2015. Le nombre d’effets secondaires est passé de 0 à 98 chez 106 patientes au total.
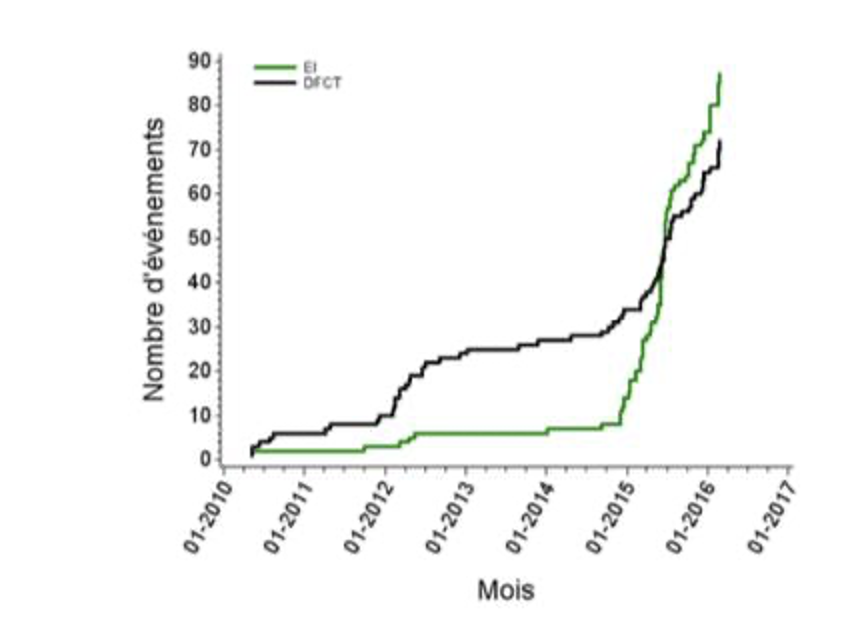
Taux d’incidence cumulé des effets secondaires et dysfonctionnements
De même, la typologie des ES fut beaucoup plus variée dans la période « après » qu’« avant » : dans la période « avant », il n’était répertorié que les dysfonctionnements propres aux prothèses (principalement représentés par les ruptures) et aucun effet secondaire n’était signalé, contre 98 « après ».
|
RPP |
28 |
29% |
|
Douleur sur prothèse |
21 |
22% |
|
Épanchement liquidien |
15 |
15% |
|
Aspect cutané inflammatoire |
10 |
10% |
|
Changement de consistance |
5 |
5% |
|
Infection sur prothèse |
4 |
4% |
|
Siliconome |
4 |
4% |
|
LAGC |
3 |
3% |
|
Eczéma |
2 |
2% |
|
Sensation de froideur |
1 |
1% |
|
Siliconome |
4 |
4% |
|
Exposition de prothèse |
1 |
1% |
|
Ganglion imprégné de silicone |
1 |
1% |
|
Calcification |
1 |
1% |
|
Brûlure cutanée à la chaleur |
1 |
1% |
|
Adénopathie axilliaire |
1 |
1% |
Typologie des effets secondaires
Le recueil de PROs permet donc d’estimer pleinement, en quantité et en qualité, des ES qui, s’ils ne sont répertoriés que par les médecins, sont sous-estimés.
D’autres études ont aussi montré que la prise en compte des PROs provenant de patientes opérées en chirurgie mammaire reconstructrice pouvait permettre aux patientes de mieux choisir la technique chirurgicale parmi plusieurs proposées par le médecin. Par l’utilisation d’un questionnaire de qualité de vie spécifique, le Breast-Q (Pusic 2009), permettant aux patientes opérées d’une reconstruction mammaire de rendre compte de leur vécu, Pusic et al. ont observé qu’aux yeux des patientes, la reconstruction mammaire autologue semblait apporter plus de satisfaction mais une moins bonne intégrité du schéma corporel que la reconstruction prothétique (Pusic JCO 2017).
Si le recueil prospectif des PROs issu de la surveillance proactive des patientes est important en reconstruction mammaire, il l’est aussi en chirurgie de résection tumorale du sein.
En effet, des interventions telles que les tumorectomies ou mastectomies sont souvent considérées comme mineures, par rapport à la reconstruction mammaire, en terme de durée, de douleur et de récupération post-opératoires. Cependant, le point de vue de la patiente n’ira pas forcément dans le même sens que celui du médecin.
A première vue, il peut paraître évident qu’un traitement conservateur de type tumorectomie associé à une radiothérapie soit plus acceptable par les patientes que la mastectomie (Engel J. Breast J, 2004).
Étonnamment, la tendance actuelle est que le choix des patientes, en Europe et en Amérique du Nord, se porte plus volontiers vers la mastectomie (y compris sur le sein controlatéral, sain, même hors mutation BRCA) chez les patientes éligibles à un traitement conservateur (Hwang ES, JCO, 2016, Kummerow, JAMA Surg, 2015). Ceci s’explique, en partie, parce que les patientes ont peur de la récidive (Fischer CS, Ann Surg Oncol 2012) et veulent éviter une radiothérapie.
Lorsque le choix de traitement est proposé aux patientes, ce qui n’est pas systématique, des outils d’aide à la décision peuvent être utilisés. Ils permettent de faire, point par point, les avantages et inconvénients en cas de tumorectomie versus mastectomie.
En cas de mastectomie, la même démarche peut être proposée pour choisir entre une reconstruction immédiate autologue ou par prothèse ou mastectomie sans reconstruction.
Concernant le type de reconstruction, de nombreuses études ont permis de progresser dans la décision grâce à des questionnaires spécifiques incluant le ressenti des patientes tels que le Breast-Q (Pusic 2009). Par contre, il existe très peu de données (Atisha DM, Ann Surg, Oncol, 2014) sur le vécu des patientes prises en charge par tumorectomie ou par mastectomie sans reconstruction.
De même, lorsqu’il s’agit du choix, pour une chirurgie conservatrice mammaire, entre une tumorectomie simple ou une oncoplastie, les PROs vont à l’encontre de ce que les médecins auraient prévu initialement. L’oncoplastie, qui fait appel à des techniques de chirurgie plastique pour réaliser l’exérèse de la tumeur est, plus complexe et implique des cicatrices plus importantes que la tumorectomie. En outre, elle exige généralement une symétrisation du sein contro-latéral. Malgré cela, la mesure des PROs semble montrer une meilleure satisfaction des patientes et moins d’effets secondaires de la radiothérapie chez les patientes ayant pu choisir l’oncoplastie avec réduction mammaire bilatérale (Di Micco, EJSO).
Par ailleurs, les patientes présentant une mutation BRCA, qui ont un risque de cancer du sein élevé, doivent choisir entre la mastectomie et la conservation du sein avec surveillance rapprochée. Pour faire ce choix, en fonction des possibilités de reconstruction et la qualité du résultat attendu par le chirurgien, il existe déjà des sites internet dédiés permettant d’avoir accès aux témoignages de patientes et/ou d’échanger avec des patientes-relais à travers les associations de patientes. Le recueil exhaustif des PROs complèterait le panel d’information, pour aider à la décision.
Enfin, deux événements récents et très médiatisés ont soulevé l’urgence de la mise en place d’un enregistrement prospectif des événements indésirables, surtout après mise en place de PMS : « l’affaire » PIP où le signalement tardif et, pour beaucoup, rétrospectif des dysfonctionnements et effets indésirables des prothèses déficientes a amené au scandale sanitaire connu (rapport ANSM PIP 2014), et la survenue de lymphome anaplasique à grandes cellules.
En effet, cette pathologie, dont la pathogénie n’est pas élucidée (Brody G, Plast Rec Surg 2014), même si le procédé de texturation des PMS semble impliqué (Loch-Wilkinson, Plast Rec Surg, 2017), a pour point d’appel principal une augmentation de volume du sein (par épanchement liquidien, ou « sérome » périprothétique). Cet exemple montre que tout effet rapporté par les patientes doit être pris en compte, contrairement à ce que peuvent avoir tendance à faire les médecins, qui se focalisent sur les effets indésirables « graves » (Atkinson 2016).